Dạng5_Nhậnbiet_Tiếp_5
Tóm tắt ngắn:
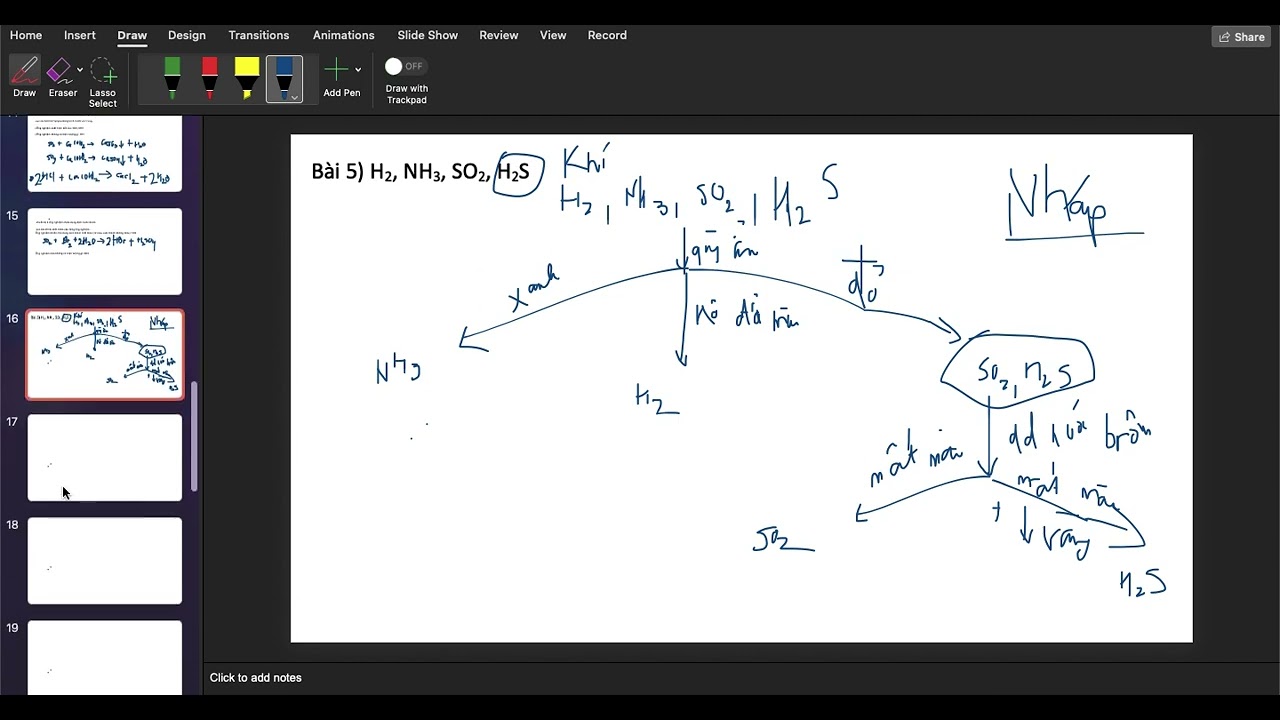
- Video hướng dẫn nhận biết 4 khí H2, NH3, SO2, H2S bị mất nhãn bằng phương pháp hóa học.
- Điểm mấu chốt là sử dụng giấy quỳ tím để phân biệt tính axit/bazơ, sau đó dùng dung dịch nước brom để phân biệt SO2 và H2S dựa trên hiện tượng mất màu và tạo kết tủa vàng.
- Phương pháp này áp dụng trong phòng thí nghiệm để nhận biết các chất khí. Việc sử dụng mùi để nhận biết bị loại bỏ vì lý do an toàn.
- Các quá trình được mô tả chi tiết bao gồm: sử dụng giấy quỳ tím, phản ứng của các khí với nước, và phản ứng của SO2 và H2S với nước brom.
Tóm tắt chi tiết:
Video được chia thành các phần chính sau:
Phần 1: Giới thiệu và phương pháp tổng quan: Video giới thiệu bài toán nhận biết 4 khí H2, NH3, SO2, H2S. Giảng viên nhấn mạnh việc không sử dụng khứu giác để nhận biết vì lý do an toàn. Phương pháp chính được đề xuất là sử dụng giấy quỳ tím để phân loại dựa trên tính axit/bazơ.
Phần 2: Sử dụng giấy quỳ tím: Giấy quỳ tím sẽ hóa xanh với NH3 (do tạo NH4OH), hóa đỏ với SO2 và H2S (do tạo H2SO3 và dung dịch H2S), và không đổi màu với H2. Giảng viên giải thích phản ứng của NH3 và nước tạo NH4OH (bazơ yếu), và phản ứng của SO2 và H2S với nước tạo axit yếu tương ứng.
Phần 3: Phân biệt SO2 và H2S: Đây là phần khó nhất. Cả SO2 và H2S đều làm mất màu dung dịch nước brom. Tuy nhiên, chỉ có H2S tạo thêm kết tủa vàng (lưu huỳnh). Giảng viên giải thích chi tiết phản ứng của SO2 và H2S với nước brom, nhấn mạnh sự khác biệt về sản phẩm tạo thành: H2SO4 (SO2) và lưu huỳnh (H2S). "Nếu mà dung dịch bị mất màu, thì sẽ là khí SO2; còn nếu dung dịch bị mất màu và kết tủa vàng thì đó chính là khí H2S".
Phần 4: Tổng kết và minh họa: Giảng viên tóm tắt lại toàn bộ quá trình, minh họa bằng cách vẽ sơ đồ và viết phương trình phản ứng cho từng bước. Ông nhắc lại tầm quan trọng của việc ghi chép các phản ứng vào nháp trước khi trình bày. Ông cũng nhắc đến các phương pháp khác như nhận biết mùi (tuy nhiên không khuyến khích vì lý do an toàn). "Trong thực tế trong phòng thí nghiệm ấy thì chỉ cần hít phải một cái lượng nhỏ khí đó thôi thì có thể nguy hiểm đến sức khỏe Và thậm chí là nguy hiểm đến tính mạng em nhá."
Tóm lại, video cung cấp một hướng dẫn chi tiết và dễ hiểu về cách nhận biết 4 khí H2, NH3, SO2, H2S bằng phương pháp hóa học, nhấn mạnh tính an toàn và sự chính xác trong quá trình thực nghiệm.